Гиперхромия ядер — патологическое состояние, при котором увеличивается окрашиваемость клеточных ядер. Это может быть важным диагностическим признаком различных заболеваний. В статье рассмотрим причины и механизмы гиперхромии, а также ее значение в клинической практике. Понимание этого явления поможет врачам точнее интерпретировать результаты лабораторных исследований и выявлять отклонения в состоянии здоровья пациентов.
Гиперхромия → гиперхромная анемия
Возможно, к моменту, когда врач начнет анализировать мазок, о наличии избыточного насыщения гемоглобином в красных кровяных клетках и изменении их окраски уже «сообщит» цветовой показатель (ЦП).
При гиперхромии цветовой показатель будет выше 1,1 – это предел нормы ( нормохромия: ЦП – 0,85 – 1,05). Эритроцитарные индексы (MCH, MCHC), рассчитанные с помощью гематологического анализатора, также не останутся без внимания.
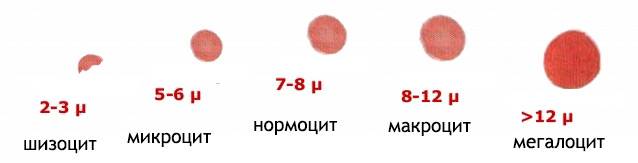
Гиперхромия является основным лабораторным признаком гиперхромных анемий и чаще всего наблюдается в сочетании с макроцитозом (гиперхромная макроцитарная анемия). В первую очередь к таким состояниям относятся авитаминоз В12 и дефицит фолатов (фолиевой кислоты – витамина B9). Эти состояния являются типичными представителями гиперхромных макроцитарных (мегалобластных) анемий. Почему именно мегалобластные? Потому что клетки значительно увеличены в размерах и представлены мегалобластами и мегалоцитами, а их диаметр (>10 мкм) значительно превышает размер макроцитов (клетки диаметром 7-8 мкм – нормоциты, более 8 мкм – макроциты, менее 7 мкм – микроциты). Таким образом, мегалобластная анемия подразумевает макроцитарную, но не каждая макроцитарная анемия является мегалобластной.
Таким образом, при морфологическом анализе образцов крови, взятых у пациентов с гиперхромной макроцитарной анемией, можно выявить:
- Красные кровяные клетки, насыщенные гемоглобином настолько, что он (Hb) затмевает центральное просветление – гиперхромия (гиперхромазия);
-
Диаметр эритроцитов превышает 10 мкм (макроциты и мегалоциты);
-
Наблюдаются фрагменты красных кровяных телец (шизоцитоз), анизоцитоз (что подтверждается автоматической обработкой пробы с показателями: средний объем эритроцитов – MCV, ширина распределения по объему – RDW, гистограмма), а также изменение формы эритроцитов (пойкилоцитоз);
- Часто можно встретить красные клетки, сохранившие ядерные структуры (тельца Жолли, кольца Кебота, полихроматофильные элементы);
- Содержание молодых форм эритроцитов – ретикулоцитов, изначально остается в пределах нормы, однако по мере прогрессирования процесса наблюдается ухудшение дифференцировки и тенденция к снижению их количества;
- При морфологическом исследовании также следует обратить внимание на изменения в белой крови: снижение количества лейкоцитов (нейтрофилов, моноцитов, эозинофилов), отсутствие базофилов и незначительное увеличение лимфоцитов. В некоторых случаях в кровь попадают молодые предшественники белых клеток – миелоциты и юные (сдвиг лейкоцитарной формулы влево);
- В тромбоцитарном звене также могут наблюдаться неестественные изменения (тромбоциты становятся гигантскими, но общее их количество – снижено).
Вся эта картина (гиперхромия, макроцитоз и сдвиг лейкоцитарной формулы) обусловлена мегалобластическим типом кроветворения в костном мозге, который является общим признаком всех анемий подобного рода (связанных с нарушением синтеза ДНК). Эти анемии могут быть как наследственными, так и приобретенными в течение жизни.
Гиперхромия ядер — это явление, которое привлекает внимание специалистов в области гематологии и онкологии. Эксперты отмечают, что гиперхромия характеризуется увеличением окрашиваемости ядер клеток, что может свидетельствовать о различных патологиях. В частности, это состояние часто наблюдается при злокачественных новообразованиях, таких как рак, а также при некоторых доброкачественных заболеваниях.
По мнению врачей, гиперхромия может быть важным диагностическим признаком, указывающим на изменения в клеточной структуре и метаболизме. Однако, как подчеркивают эксперты, для точной интерпретации этого явления необходимо учитывать контекст и сопутствующие клинические данные. Важно проводить комплексное обследование, чтобы определить истинные причины гиперхромии и выбрать соответствующую тактику лечения.

Все начинается в костном мозге
Гиперхромная макроцитарная анемия является следствием мегалобластического типа кроветворения. Что все это значит – можно показать на примере В12-дефицитной анемии. Итак:
- В костном мозге (КМ) отмечается высокая клеточность (по причине присутствия огромного количества элементов, содержащих ядро), мегалобластическое кроветворение и неэффективный эритропоэз;
- Деление клеток, которые в будущем должны стать полноценными эритроцитами на этой стадии (см. выше) нарушается, они, в значительной степени меняя свои размеры (становятся мегалобластами), изменяют и структуру (нежно-сетчатое ядро, созревает, как и цитоплазма, разновременно);
- В популяции созревающих мегалобластов, в зависимости от активности кроветворного процесса в КМ, отмечается заметная изменчивость: одни клетки более зрелые, другие – менее. И если на этом этапе в костном мозге подавляющее большинство будущих красных кровяных телец представлено промиелобластами или базофильными клетками, то специалисты говорят о «синем» КМ;
- Отличительной чертой этих огромных клеток является раннее насыщение их цитоплазмы при нетронутом нежном ядре хроматопротеином (гемоглобинезация цитоплазмы – так вот откуда берет начало гиперхромия?);
- Вместе с тем, в ядрах происходят заметные дегенеративные процессы (митозы, распад клеточного ядра), что придает им уродливость и, соответственно, неполноценность – такие клетки долго не живут, большинство из них так и не добираются до зрелого состояния («умирают» на месте «рождения» в «младенчестве»);
- Из оставшихся предшественников эритроцитов образуются мегалоциты (жизнь их также коротка) и макроциты (которые впоследствии станут определяющим лабораторным признаком гиперхромной макроцитарной анемии);
- Следует отметить, что нарушение клеточного деления оставляет синтез красного пигмента на нормальном уровне, от этого страдает только сам процесс образования красных клеток крови (разрушение ядер, распад мегалобластов – усиленный, неэффектиный эритропоэз);
- Дефицит витамина В12 приводит к тому, что появляются изменения и со стороны белой крови (нарушение синтеза ДНК идет синхронно во всех клетках). Предшественники «взрослых» лейкоцитов (промиелоциты, миелоциты, юные и палочки), а также зрелые сегментоядерные меняют свои размеры, в иных случаях нарушения касаются и тромбоцитарного звена, что объясняет изменение картины крови у больных, страдающих гиперхромной макроцитарной анемией.
Кстати, изменения в периферической крови и в костном мозге при фолиеводефицитной анемии аналогичны таковым при авитаминозе В12, ведь в синтезе пуриновых оснований, без которых в правильном направлении не идет построение ДНК, фолиевая кислота тесно «сотрудничает» с витамином B12.
| Признак | Описание | Клиническое значение |
|---|---|---|
| Гиперхромия ядра | Увеличение интенсивности окрашивания ядра клетки, обусловленное повышенным содержанием ДНК и/или конденсацией хроматина. | Часто ассоциируется с атипией клеток и может быть признаком злокачественного новообразования. |
| Причины гиперхромии | Увеличение количества хроматина (полиплоидия, анеуплоидия), конденсация хроматина, нарушение метаболизма ДНК, воспалительные процессы. | Помогает в дифференциальной диагностике между доброкачественными и злокачественными изменениями. |
| Методы выявления | Гистологическое исследование (окраска гематоксилином и эозином), цитологическое исследование. | Основной метод диагностики в патологической анатомии и цитологии. |
| Степень выраженности | Может быть легкой, умеренной или выраженной. | Выраженная гиперхромия чаще указывает на высокую степень злокачественности. |
| Сопутствующие изменения | Плеоморфизм ядер, увеличение ядерно-цитоплазматического соотношения, наличие атипичных митозов, неровность контура ядра. | Комплексная оценка всех морфологических признаков важна для точной диагностики. |
Интересные факты
Гиперхромия ядер — это термин, который используется в гистологии и цитологии для описания увеличенной окрашиваемости клеточных ядер, что может указывать на различные патологические состояния. Вот несколько интересных фактов по этой теме:
-
Признак злокачественности: Гиперхромия ядер часто наблюдается в опухолевых клетках. Увеличенная окрашиваемость ядер может свидетельствовать о повышенной активности синтеза ДНК и клеточном делении, что является характерным признаком злокачественных новообразований.
-
Связь с другими изменениями: Гиперхромия ядер часто сопровождается другими морфологическими изменениями, такими как увеличение размера ядер (анизоцитоз) и изменение формы ядер (анизокариоз). Эти изменения могут помочь в диагностике различных заболеваний, включая рак.
-
Диагностические методы: Для выявления гиперхромии ядер используются различные методы окраски, такие как гематоксилин-эозин, которые позволяют визуализировать изменения в клетках под микроскопом. Это важно для патоморфологической диагностики и определения стадии заболевания.
Эти факты подчеркивают важность гиперхромии ядер в медицинской диагностике и патологии.

Очень кратко о причинах и симптомах
Анемия не является конкретной болезнью, а представляет собой клинический синдром, свидетельствующий о хроническом недостатке кислорода в организме. Однако это состояние может привести к более серьезным заболеваниям, таким как ишемическая болезнь сердца (ИБС) и сердечная недостаточность, которые сложно игнорировать.
Поэтому причины анемического синдрома вызывают особый интерес. Рассмотрим состояния, которые характеризуются лабораторным показателем, известным как гиперхромия:
- Авитаминоз В12 возникает из-за недостатка цианокобаламина в рационе, нарушений всасывания в кишечнике, конкуренции с паразитами, а также из-за проблем с поджелудочной железой и других заболеваний желудочно-кишечного тракта. Некоторые случаи В12-дефицитного состояния могут передаваться по наследству;
- Фолиеводефицитная анемия чаще всего затрагивает вегетарианцев, пожилых людей, страдающих алкоголизмом, а также женщин в период беременности;
- Мегалобластная анемия с гиперхромией возникает при нарушении работы ферментов, отвечающих за синтез пуриновых и пиримидиновых оснований, что, в свою очередь, нарушает синтез ДНК и РНК;
- Гиперхромия (и макроцитоз) может быть следствием серьезных заболеваний печени, которые приводят к значительным нарушениям в витаминах, так как именно в печени накапливаются многие витамины, включая В12 и В9, участвующие в синтезе пуриновых и пиримидиновых оснований;
- Появление гиперхромии в красных кровяных тельцах может наблюдаться при миелодиспластическом синдроме или некоторых формах гемолитических анемий, однако этот признак не всегда является стабильным и зависит от стадии и формы заболевания.
Кроме того, гиперхромия может возникать из-за кислородного голодания, особенно у людей, активно курящих. Организм курильщика, испытывающий постоянную гипоксию, может реагировать на это состояние подобным образом. Известно, что у курильщиков уровень гемоглобина в крови выше, чем у тех, кто не курит, хотя это скорее относится к эпизодической гиперхромии, а не к гиперхромной анемии.
Что касается симптомов, то мегалобластные (макроцитарные) гиперхромные анемии проявляются:
- общими симптомами, характерными для всех подобных состояний (слабость, головные боли, бледность, тахикардия);
- и специфическими симптомами (жжение языка, неуверенная походка).
При В12-дефицитной анемии страдают кровь, желудочно-кишечный тракт и нервная система (триада синдромов), в то время как для фолиеводефицитного состояния изменения в нервной системе не характерны. Однако на практике чаще всего встречается комбинированный вариант: В12-фолиеводефицитная анемия, симптомы и причины которой, а также диагностика, подробно описаны в соответствующей публикации (В12-дефицитная и фолиеводефицитная анемия).
Как лечить гиперхромию?
Лечение отдельно гиперхромии, конечно, не предусмотрено. Лечат авитаминоз В12, фолиеводефицитное состояние или (что чаще бывает) – В12-фолиеводефицитную анемию.
Лечение фолиеводефицитной анемии состоит в назначении препаратов витамина В9 (витамин В9 – это и есть фолиевая кислота). Однако следует проявлять осторожность, если нет уверенности, что это именно фолиеводефицитная анемия, потому что применение в подобных случаях витамина В9 может обернуться неприятностями. Болезнь, не связанная с дефицитом фолатов, не только не отступит, а еще больше начнет проявлять себя. В этих ситуациях более оправдано назначение цианокобаламина.
Лечение самого авитаминоза В12 стоит на трех принципах:
- Дать организму цианокобаламина вволю;
- Постоянно, не переставая, пополнять запасы недостающего витамина;
- Всеми силами стараться предотвратить развитие анемии, иначе потом с ней тяжело будет справиться.
Вот и все, что вкратце можно сказать о лечении двух гиперхромных макроцитарных анемий (или одного – сочетанного варианта). Кстати, более подробную информацию можно найти на одной из страниц нашего сайта в той же публикации, о которой сообщалось выше (В12-дефицитная и фолиеводефицитная анемия).
И напоследок касательно терапии. Чтобы от лечения пошел прок, пациент не должен забывать о потребностях своего организма в отношении витаминов и обогащать свой рацион продуктами, их содержащими.
Злокачественная опухоль — новообразование, характеризующееся агрессивным течением, общим неблагоприятным влиянием на обменные процессы в организме, способностью рецидивировать и давать метастазы.
Классификация.
По степени дифференцировки различают злокачественные опухоли:
- высокодифференцированные, то есть максимально приближающиеся по гистологической картине к строению нормальной ткани,
- среднедифференцированные,
- низкодифференцированные.
Злокачественные опухоли бывают:
- солидными (с наличием опухолевого узла),
- диффузными, к каковым относятся лейкозы.
Чем ниже дифференцировка, тем хуже прогноз. Опухоли, клетки которых утрачивают всякое сходство с теми или иными нормальными клетками, в результате чего при световой микроскопии невозможно определить ткань, из которой они происходят, называются анапластическими.
В отношении конкретной злокачественной опухоли клиницистов интересуют два аспекта: степень ее злокачественности по гистологическим признакам (grade) и ее стадия по распространенности за пределы первичного узла (stage).
Злокачественные эпителиальные опухоли обозначают термином “рак” (син.-карцинома). Злокачественные опухоли из тканей мезенхимального происхождения обозначают термином “саркома”.
Раки делятся на:
- неинвазивные (син.- рак на месте, carcinoma in situ),
- не прорастающие за пределы базальной мембраны,
- инвазивные, то есть с разрушением базальной мембраны.
Если лечение начинается, когда рак уже оказывается инвазивным, прогноз значительно хуже.
По соотношению эпителиального и стромального компонентов раки также делятся на
- мягкие (син.- медуллярный рак, рак-мозговик), в которых строма развита слабо, и
- плотные (син. — скиррозные), в которых строма преобладает над собственно опухолевой тканью.
Встречаемость.
Злокачественные опухоли, к сожалению, — явление распространенное. Вероятность их возникновения в организме резко увеличивается с возрастом. Частота тех или иных злокачественных опухолей сильно варьирует не только в разных странах, но даже в разных районах одной и той же области.
Условия возникновения.
Условием развития злокачественных опухолей является утрата организмом контроля за постоянством антигенного состава и его неспособность элиминировать и предотвращать размножение атипичных клеток-мутантов.
Механизмы возникновения.
Иммунитет — это не только невосприимчивость к инфекции, как это рассматривалось раньше, но более широкое понятие, включающее контроль за антигенным постоянством внутренней среды организма. В процессе деления клеток постоянно возникают в небольших количествах чужеродные в антигенном отношении несвойственные организму клетки-мутанты, которые распознаются иммунной системой и уничтожаются.
Под действием ряда факторов — некоторых вирусов, химических канцерогенов, лучевых и других воздействий — увеличивается, с одной стороны, количество клеток-мутантов, а с другой стороны, возникает недостаточность иммунной системы, при которой она оказывается неспособной распознавать и уничтожать чужеродные, не соответствующие генетической программе организма клетки. Эти клетки начинают бесконтрольно размножаться, образуя злокачественную опухоль.
Макроскопическая картина.
Сравнительная характеристика типичных макроскопических признаков доброкачественных и злокачественных опухолей.
Микроскопическая картина.
Помимо свойственного для всех типов опухолей тканевого атипизма, для злокачественных характерен еще и клеточный атипизм. В это понятие входят:
- Клеточный полиморфизм — наличие в опухоли клеток разной величины и формы. Реже, например, при гемобластозах, в многослойном плоском эпителии, признаком клеточного атипизма является их мономорфизм — несвойственное ткани однообразие клеток.
- Ядерный полиморфизм — наличие в клетках ядер различной величины и формы.
- Гиперхромия ядер — более интенсивное их окрашивание ядерными красителями.
- Увеличение ядерно-цитоплазматического соотношения — основная функция злокачественной опухолевой клетки — размножение, поэтому ядро занимает больший удельный объем;
- Многочисленные митозы.
- Атипичные митозы.
- Гистохимический атипизм — появление в цитоплазме опухолевой клетки нетипичного в обычных условиях вещества, например, слизи.
Помимо перечисленных, выявляемых при световой микроскопии признаков, существуют и другие признаки клеточного атипизма:
- ультраструктурный атипизм,
- биохимический атипизм,
- антигенный атипизм.
Характерной микроскопической картиной, отражающей злокачественный характер опухоли, является ее врастание в сосуды и в соседние ткани.
Клиническое значение.
- Сопровождаются так называемой раковой кахексией, основной чертой которой является истощение, связанное с активизацией процессов катаболизма жиров и белков, поскольку опухоли для ее жизнедеятельности нужны пластические материалы и энергетический субстрат.
- Сопровождаются паранеопластической анемией, связанной с подавлением эритропоэза биологически активными веществами, циркулирующими в крови в высоких концентрациях.
- Замещение опухолевой тканью большей части органа ведет к недостаточности его функции.
- Сдавление опухолью прилежащих тканей, может вызвать в них ишемию и некроз.
- Разъедание опухолью крупных сосудов проявляется кровотечениями.
- Разрастание злокачественной опухоли в стенке полого органа может привести к его разрыву.
Наиболее частыми непосредственными причинами смерти при злокачественных опухолях бывают: острая пневмония, анемия, кахексия, поражение метастазами жизненноважных органов, сердечная недостаточность.
Злокачественные опухоли молочной железы, как причина смертности от онкологических заболеваний среди женщин, занимают первое место как в России, так и в мире. Это также основная причина смерти среди женщин старше 40 лет. Примерно у 8% женщин (одной из 13) в течение жизни развивается злокачественная опухоль молочной железы. К сожалению, отмечается тенденция к росту заболеваемости и смертности от рака молочной железы, особенно выраженная в странах с высоким уровнем жизни. Так, в странах Северной Европы, Северной Америки и Австралии заболеваемость составляет 70-90 вновь выявленных случаев злокачественных опухолей на 100 000 населения в год (ВОЗ, 2003). Около 90% злокачественных опухолей молочной железы составляет рак, реже встречаются неэпителиальные опухоли.
Факторы риска рака молочной железы
- Возраст: чаще диагностируется у женщин старше 40 лет.
- Генетические особенности: наиболее часто предрасположенность передается по материнской линии, имеет значение мутация генов ВRСА и ВRСА 2.
- Диагностированный ранее рак, особенно дольковый, в одной молочной железе.
- Избыточная жировая клетчатка, особенно при быстром наборе веса, в сочетании с гиперплазией эпителия протоков.
- Раннее начало менструаций (ранее 12 лет) и позднее их окончание (после 50 лет).
- Чаще рак развивается у женщин без детей или не кормивших детей. В норме инволюция молочной железы происходит только после вскармливания ребенка грудью; если женщина не кормила грудью, чаще развиваются гиперпластические и диспластические процессы.
- Пролиферативная форма фиброзно-кистозной болезни.
- Нарушение гормонального баланса: длительное лечение гормонами, особенно эстрогенами, активные опухоли яичника, эндометрия и щитовидной железы, гормональная контрацепция при неправильном применении и гормональная заместительная терапия в климактерическом периоде.
- Питание: так называемая «западная» диета -высококалорийная с наличием большого содержания жиров, «красного» мяса, особенно жареного, и малым содержанием растительной клетчатки, постоянное употребление алкоголя в значительном количестве.
- Рентгеновское облучение: ткань молочной железы в 30-49 лет наиболее подвержена действию рентгеновских лучей
Клинические проявления
Клинические признаки могут отсутствовать, или имеется лишь один из признаков, или их различное сочетание:
- Уплотнение в молочной железе.
- Болезненность в молочной железе или в подмышечной области.
- Кожные симптомы (отек, покраснение, «симптом «лимонной корки»).
- Втяжение соска.
- Опухолевидные образования в подмышечной области
Факторы, влияющие на прогноз заболевания
- Распространенность процесса. Лучшим прогнозом отличается ранний рак (неинфильтративный дольковый или протоковый, рак Педжета или инвазивный, рак размером до 1 см и без метастазов в регионарных лимфатических узлах). Наличие опухоли больших размеров в момент установления диагноза является признаком неблагоприятным. При установлении диагноза на стадии распространенного рака с поражением лимфатических узлов (особенно если имеется более четырех пораженных лимфатических узлов) и других органов отмечен плохой прогноз. Висцеральные метастазы наиболее часто встречаются в легком, печени, костях и головном мозге, могут поражаться и другие органы.
- Гистологические особенности. Медуллярный, папиллярный и слизистый рак отличается лучшим прогнозом по сравнению с другими формами рака: реже поражаются лимфатические узлы, больше продолжительность жизни. При дольковом раке прогноз хуже, чем при протоковом. Увеличенное число гистиоцитов в лимфатических узлах, наличие плазматических клеток и лимфоцитов в ткани, окружающей опухоль, сочетается с более благоприятным прогнозом.
- Возраст при установлении диагноза. Прогноз у женщин пожилого возраста лучше, чем у молодых с аналогичной опухолью и стадией процесса.
- Особенности организма. Рост и развитие рака напрямую зависят от взаимоотношения организма и клеток рака (иммунного статуса, гормонального фона и проч.).
- Рецепторы эстрогенов и прогестерона. Примерно у половины больных в опухоли молочной железы имеются рецепторы эстрогенов — белки, способные связывать эстрадиол. Более чем у половины больных с наличием эстрогенных рецепторов имеется ремиссия после гормонального лечения рака, а среди пациенток с отсутствием рецепторов лишь единичные «отвечают» на гормональную терапию (см. раздел Опухолевые маркеры при раке молочной железы). Наличие рецепторов прогестерона в опухоли также сочетается с лучшим ответом на гормональную терапию.
Врач, устанавливающий морфологический диагноз рака, должен отдавать себе отчет в том, что этот диагноз может служить основанием к началу, как правило, тяжелого лечения (хирургического, лучевого, химиотерапевтического и проч.).
Рак молочной железы: общие цитологические признаки
- Клеточный и ядерный полиморфизм:
- разные размеры и форма клеток и ядер;
- неровные контуры ядерной мембраны;
- неравномерное распределение хроматина;
- грубый хроматин;
- глыбчатая и грубоглыбчатая структура хроматина;
- ядрышки разных размеров и формы
- Разрозненное (рыхлое) расположение клеток (что обеспечивает их попадание в лимфоотток, кровь)
- обильный клеточный состав;
- отсутствие упорядоченности расположения клеток в структурах (комплексах);
- разрозненное расположение клеток с сохранившейся цитоплазмой
- Дегенеративные изменения клеток и ядер
- Нарушение ядерно-цитоплазматического соотношения
Цитологические признаки отдельных форм рака молочной железы
- Протоковый рак
- Тубулярный рак
- Дольковый рак
- Медуллярный ракМедуллярный рак (5-7%) молочной железы не является синонимом рака со слабым развитием стромы и не аналог медуллярного рака щитовидной железы.
- Гистологические особенности
- Цитологические особенности
- Папиллярный ракВстречается в 1-2% инвазивного рака молочной железы и отличается благоприятным клиническим течением.
- Гистологические особенности
- Цитологические признаки
- Рак ПеджетаХарактеризуется экземоподобным поражением кожи соска и околососковой зоны. Составляет около 1-4,5% злокачественных опухолей молочной железы.
- Гистологические особенности
- Цитологические признаки
- Слизистый рак (муцинозный, коллоидный)Слизистый рак встречается в 2-5% рака молочной железы, характеризуется внеклеточной продукцией слизи. Макроскопически опухолевый узел четко отграничен от окружающих тканей и более мягкой консистенции, чем типичный узел рака.
- Гистологические особенности
- Цитологические признаки
- Апокриновый ракОтносится к редкой форме рака. В молочной железе апокринизация нередко встречается как при доброкачественных процессах (кисты, склерозирующий аденоз, фиброаденома, внутрипротоковая папиллома), так и при раке, но апокриновый рак можно диагностировать, если апокриновые клетки составляют не менее 75% объема опухоли.
- Гистологические особенности
- Цитологические признаки
- Плоскоклеточный ракПлоскоклеточный рак встречается редко, обычно в пожилом возрасте. Клинические проявления сходны с признаками протокового рака, однако опухоль может иметь большие размеры в связи с присутствием в ней кистозной полости. При пункции в этом случае получают густую жидкость желтоватого цвета.
- Гистологические особенности
- Цитологические признаки
- Скиррозный рак (скирр)Не является «особой» формой рака, а отличается некоторыми клеточными и структурными особенностями:
- очень плотная и клеточная строма;
- клетки мелкие (трудно отличить от гиперплазии с атипией);
- клетки располагаются небольшими структурами;
- выраженная гиперхромия ядер.
- СаркомаОпухоль развивается из мезенхимальной ткани молочной железы, составляет около 1% злокачественных опухолей.
Злокачественная листовидная опухоль
Пограничная листовидная опухоль. Чаще встречается у пожилых женщин. Клинически проявляется как быстро растущая опухоль.
- Гистологические особенности
- Цитологические признаки
Метастазы в молочной железе
Вторичные опухоли встречаются редко. Первичным очагом может быть лейкоз, лимфома, меланома, рак легкого, эндометрия и др.
Рак
Рак из недифференцированных клеток фолликулярного эпителия. Этот тип рака характеризуется клетками, которые частично или полностью утратили свою структурную и функциональную дифференциацию, а также имеют высокий митотический индекс (7-21%). В рамках этого типа выделяют две подгруппы цитологических картин.
А. Круглоклеточный рак. В цитологических образцах опухоль проявляется наличием незрелых клеток, которые утратили сходство с тиреоидным эпителием. Эти клетки напоминают ретикулярные, но отличаются большей величиной и полиморфизмом. Лимфоидоподобные элементы, как правило, однотипны и меньше по размеру. В большинстве случаев в цитограммах одновременно присутствуют оба типа клеток, но в разных пропорциях. Ядра этих клеток крупные, занимают почти всю клеточную площадь и расположены в центре. Форма ядер может быть округлой, слегка лапчатой или бобовидной, с небольшими вдавлениями. Хроматин окрашен диффузно и может иметь различные формы, от тонкосетчатого до мелких пылевидных зерен, плотно заполняющих ядро.
Цитоплазма клеток однородная: у одних она широкая и четко контурирована, у других — узкая и базофильная. Клетки располагаются разрозненно, иногда образуя скопления, где они, адаптируясь по форме, обтекают друг друга, что создает видимость эпителиальной структуры. Появление таких мелких фрагментов клеток, «сцементированных» между собой, может свидетельствовать о раке. Определить гистологическую форму опухоли в данном случае сложно, так как необходимо провести дифференциальный диагноз между ретикулолимфосаркомой и ангиосаркомой.
Б. Полиморфноклеточный рак отличается выраженной атипичностью всех клеточных элементов, а также наличием гигантских одноядерных и многоядерных клеток с полиморфными ядрами и множественными митозами. Цитограммы имеют характерные волокнистые межуточные структуры (коллагеновые и преколлагеновые волокна). Клетки могут иметь разнообразные формы (вытянутые, веретенообразные, округлые, полигональные) и размеры (от мелких до гигантских). Ядра крупные, могут быть округлыми, палочковидными, овальными или веретенообразными, а их хроматин может быть тяжистым, глыбчатым или пылевидным.
Признаком анаплазии служат гипертрофированные ядрышки, часто множественные. Гигантские ядрышки могут нарушать соотношение ядрышка и ядра. Цитоплазма клеток окрашена в различные оттенки, от светло-голубых до ярко базофильных. Розоватые оттенки, характерные для раковых клеток щитовидной железы, обычно отсутствуют.
Клетки располагаются разрозненно, иногда образуя тяжи или синцитии без четких границ. В некоторых случаях между клетками имеются прослойки волокнистой субстанции, что создает видимость эпителиальной структуры. Когда клеточные тяжи плотно окружены фиброзной стромой, цитограммы могут напоминать веретеноклеточный рак. Клетки таких опухолей обычно небольшие, слегка вытянутые и содержат мелкие гиперхромные ядра.
Если в препаратах преобладают гигантские клетки, можно предположить гигантоклеточный рак. Общее количество крупных и гигантских клеток может достигать 50-70%. Чаще всего встречаются округлые элементы с гигантскими ядрами. Клетки располагаются разрозненно или образуют обширные синцитии. Такие клетки могут секретировать по апокриновому типу, их цитоплазма окрашена в отчетливый розоватый цвет и содержит мелкие коллоидные включения.
В цитограммах полиморфноклеточного и гигантоклеточного рака могут встречаться атипичные клетки, напоминающие плоскоэпителиальные элементы, или даже комплексы плоскоклеточного рака. Вероятно, плоскоклеточный рак щитовидной железы является одной из форм недифференцированного рака и возникает в процессе прогрессии опухоли.
Описанные цитограммы позволяют оценить злокачественность клеток. Однако не всегда удается точно установить эпителиальную природу опухоли, особенно когда клетки становятся веретенообразными, что затрудняет диагностику. Диагностическим признаком рака является выраженный полиморфизм клеточных элементов, наличие комплексов, напоминающих железистые структуры, а также переходные формы клеток от анаплазированных до сохранивших некоторые признаки тиреоидного эпителия. Косвенным признаком рака могут служить клеточные скопления, окруженные волокнистой субстанцией, напоминающие эпителиальные фрагменты.
Рак с умеренной дифференцировкой клеток фолликулярного эпителия. Клетки рака демонстрируют выраженные признаки атипичности, но сохраняют морфологические характеристики щитовидного эпителия, включая способность к образованию специфических структур и секреторную функцию. Митотический индекс составляет 1,5-10%. Выделяются две подгруппы цитопатологических картин.
А. Фолликулярно-папиллярный рак с солидным компонентом. Клетки крупные и гигантские, их ядра могут быть светлыми или гиперхромными и часто располагаются эксцентрично. Хроматин неравномерно распределен в ядре, и характерное кольцевидное расположение хроматиновых нитей напоминает рисунок «спила» дерева. В ядрах могут встречаться как одиночные, так и множественные ядрышки. Цитоплазма клеток обильная, светлая, с четко выраженным фестончатым контуром и содержит секреторные вакуоли, окрашенные в розоватые и красноватые оттенки.
В цитоплазме могут присутствовать глыбки гемосидерина и кристаллы гематоидина, что указывает на участие раковых клеток в процессе фагоцитоза. Опухоли с подобными цитограммами часто имеют кистозные полости, и при пункции можно получить значительное количество жидкости. Если клетки образуют обширные однослойные скопления, то речь идет о солидном раке щитовидной железы. В таких случаях в цитограммах преобладают округлые и полигональные клетки с крупными ядрами.
Б. Фолликулярная аденокарцинома характеризуется обилием структур с коллоидом и почти полным отсутствием симпластов. В цитограммах железистые структуры составляют 54,7% всех клеточных образований, а папиллярные формы — лишь 12,6%. Клетки опухоли среднего размера, округлой формы, с однородной, умеренно выраженной цитоплазмой. У большинства клеток ядра содержат 1-2 мелких ядрышка. В препарате выявляется большое количество коллоида, что может напоминать цитограммы аденом.
На рак щитовидной железы указывают единичные многоядерные клеточные симпласты и клетки, сохранившие характерные черты исходной ткани. При смешанных опухолях шарообразные слизевидные массы с клетками не отражают истинные железистые структуры, а лишь имеют с ними внешнее сходство.
Рак из С-клеток (солидный рак с амилоидозом стромы). Многие исследователи выделяют рак с амилоидом в строме в отдельную гистологическую форму, связывая его происхождение с С-клетками. В цитологических препаратах обнаруживаются атипичные оксифильные клетки с обильно гранулированной цитоплазмой и нарушением межклеточных связей. Высокий митотический индекс обусловлен большим числом амитотически делящихся клеток.
Выделяются три варианта цитограмм этого типа.
а) Дифференцированный вариант. Клетки сохраняют признаки железистого эпителия, имеют средние размеры и округлую форму. Ядра клеток разного размера, окрашены интенсивно. Цитоплазма заполнена оксифильными гранулами. Клетки располагаются разрозненно и образуют структуры вокруг амилоидных масс.
б) Низкодифференцированный вариант характеризуется однотипными клетками, преимущественно округлой формы с нарушением ядерно-цитоплазматического отношения. Ядра крупные, занимают почти всю клетку. Цитоплазма узкая, окрашена в нежно-голубой цвет. Амилоид может замуровывать клетки, что приводит к потере четкости контуров.
в) Смешанный вариант состоит из полиморфных клеток без признаков секреции, но сохранивших формообразовательную функцию. Ядра клеток гиперхромные, содержат гипертрофированные ядрышки. Присутствие двухъядерных клеток является важным признаком амилоидного рака.
Рак из клеток Ашкинази (Гюртле). Характеризуется выраженными критериями злокачественности. Клетки крупные и гигантские, с разнообразной формой. Ядра клеток преимущественно округлые, часто гиперхромные. Цитоплазма обильно гранулированная, может иметь вид разволокненной массы. Клетки располагаются разрозненно и образуют синцитиальные образования.
Цитологический диагноз злокачественного новообразования не вызывает затруднений, однако уточнить тканевую и гистологическую форму опухоли бывает сложно. Главный признак рака из клеток Ашкинази — монотонная светлая окраска клеток и обильно гранулированная цитоплазма.
Плоскоклеточный рак. Плоскоклеточный рак щитовидной железы составляет менее 1% всех злокачественных опухолей этого органа. Его происхождение связывают с метаплазией эпителия или с остатками бранхиогенного эпителия. Плоскоклеточный рак может развиться вторично в результате метастазирования или прорастания опухоли из соседних органов. Клетки плоскоклеточного рака имеют выраженные признаки злокачественности.
Цитоморфологическая особенность опухоли заключается в том, что плоскоэпителиальные атипичные элементы всегда сопровождаются полиморфными клетками, образующими саркомоподобные структуры. Для правильного диагноза необходимо выявить элементы с классическими признаками плоскоклеточного рака. В цитограммах при ороговевающем раке клетки имеют разнообразные формы, а при неороговевающем — округлые и полигональные.
Наряду с атипичными клетками могут встречаться пролиферирующие неизмененные эпителиальные элементы. При достаточном количестве атипичных клеток диагноз рака не вызывает затруднений, однако определить первичность поражения щитовидной железы сложно.
Диагностика гиперхромии
Ядер является важным аспектом в гистопатологии и цитологии, так как она может служить индикатором различных патологических процессов в организме. Гиперхромия ядер характеризуется увеличением интенсивности окраски ядер клеток, что указывает на повышенное содержание ДНК. Это состояние может быть связано с различными заболеваниями, включая рак, воспалительные процессы и другие нарушения.
Для диагностики ядер используются различные методы, включая световую микроскопию, электронную микроскопию и специальные окраски. При световой микроскопии образцы тканей окрашиваются с использованием различных красителей, таких как гематоксилин и эозин, которые позволяют визуализировать ядерные структуры. Гиперхромные ядра будут выглядеть более темными и насыщенными по сравнению с нормальными клетками.
Электронная микроскопия предоставляет более детальное изображение клеточных структур и позволяет выявить изменения на ультраструктурном уровне. Этот метод может быть особенно полезен для изучения клеток, которые трудно оценить с помощью световой микроскопии.
Кроме того, для более точной диагностики ядер могут использоваться молекулярно-генетические методы, такие как ПЦР (полимеразная цепная реакция) и флуоресцентная гибридизация in situ (FISH). Эти методы позволяют выявить изменения в генетическом материале клеток, которые могут быть связаны с гиперхромией.
Важно отметить, что ядер не является самостоятельным диагнозом, а скорее симптомом, который может указывать на наличие различных заболеваний. Поэтому для правильной интерпретации результатов диагностики необходимо учитывать клиническую картину, анамнез пациента и другие лабораторные данные.
В заключение, диагностика ядер требует комплексного подхода и использования различных методов исследования. Это позволяет не только выявить наличие гиперхромии, но и установить ее причины, что является ключевым для выбора правильной тактики лечения и дальнейшего наблюдения за пациентом.
Вопрос-ответ
Что такое гиперхромия ядер?
Гиперхромазия — термин, который патологи используют для описания ядра клетки, которое выглядит темнее обычного при исследовании под микроскопом. Большая часть генетического материала клетки (ДНК) находится в ядре.
Что означает ядерная гиперхромазия?
Ядерная гиперхромазия 2, 9, 13. Повышение тинкториальных свойств ядра или интенсивности окраски хроматина за счет увеличения в нем содержания хроматина.
Что такое гиперхромия?
Гиперхромия, то есть увеличение среднего содержания гемоглобина в одном эритроците, дающее цветовой показатель выше единицы, зависит исключительно от увеличения объема эритроцитов, а не от повышенного насыщения их гемоглобином.
Что такое полиморфизм ядер?
Полиморфизм ядер — это способность ядерных реакторов или ядерных систем функционировать с различными типами ядерного топлива или в разных режимах работы, что позволяет оптимизировать их эффективность и безопасность. В контексте ядерной физики это может означать использование различных изотопов или комбинаций материалов для достижения желаемых характеристик реакции, таких как мощность, срок службы топлива и уровень отходов.
Советы
СОВЕТ №1
Изучите основные причины гиперхромии ядер, такие как воспалительные процессы, опухолевые изменения и генетические факторы. Понимание этих причин поможет вам лучше ориентироваться в возможных диагнозах и методах лечения.
СОВЕТ №2
Регулярно проходите медицинские обследования, особенно если у вас есть предрасположенность к заболеваниям, связанным с гиперхромией ядер. Раннее выявление может значительно повысить шансы на успешное лечение.
СОВЕТ №3
Обсуждайте результаты анализов с вашим врачом и не стесняйтесь задавать вопросы. Понимание вашего состояния и возможных последствий гиперхромии ядер поможет вам принимать более обоснованные решения о здоровье.
СОВЕТ №4
Следите за своим образом жизни: правильное питание, физическая активность и отказ от вредных привычек могут снизить риск развития заболеваний, связанных с гиперхромией ядер, и поддержать общее здоровье.